新冠病毒的武器——突变与进化
时间:2022-07-05 04:25:37 来源:科普之家 作者:biokiwi 栏目:前沿 阅读:99
在这场包括人类在内的动物与新型冠状病毒(SARS-CoV-2)之间的博弈里,人类采取了隔离、研发药物和疫苗等策略,而新冠病毒也在不断积累和孵育它们专属的武器——突变与“进化”。
从2020年12月开始,新冠病毒的变异程度似乎更上一层台阶,在英国东南部被鉴定出的新冠病毒变异毒株 B.1.1.7 表现出更快的传播速度。传染病学教授 Jeremy Farrar 在《科学》(Science)的报道中提到:“因为病毒的不断进化,一个难以预测的阶段即将到来。”
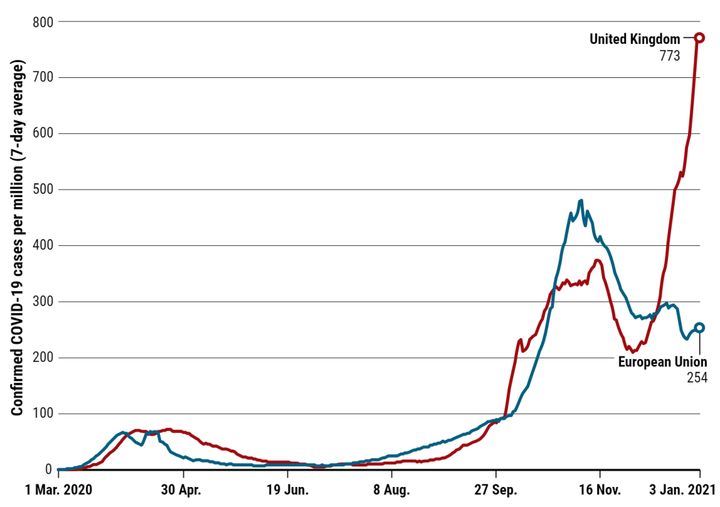 英国新冠疫情在变异毒株出现后传播速度明显加快 | JOHNS HOPKINS UNIVERSITY CSSE COVID-19 DATA
英国新冠疫情在变异毒株出现后传播速度明显加快 | JOHNS HOPKINS UNIVERSITY CSSE COVID-19 DATA
病毒为什么会突变?生物的遗传物质包含着巨大的信息量,例如人类一套遗传信息由大约30亿个碱基对(base pair,遗传信息的基本单位)排列组合构成。相比之下,新冠病毒要小得多,只有3万个碱基对左右。
尽管数量庞大,这些碱基对在复制的过程中,也还是在蛋白酶的帮助下一个一个合成的。即便有精密的“校对仪器”和严谨的“审核团队”,冗杂的复制过程难免会出现一些错误,例如放错了一个碱基、多或少合成了一段等等;再加上来自外界的辐射或有害化学物质的影响,就形成了大家有所耳闻的突变和变异。
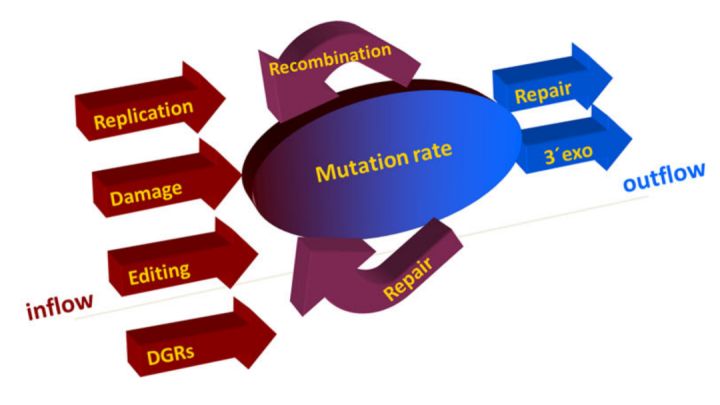 病毒突变率的定义和原因 | Sanjuán, R., Domingo-Calap, P., 2016
病毒突变率的定义和原因 | Sanjuán, R., Domingo-Calap, P., 2016
但是不同之处在于,由细胞构成的生命中,脱氧核糖核酸(DeoxyriboNucleic Acid,DNA)是主要的遗传信息载体;而病毒的世界里却存在例外,核糖核酸(RiboNucleic Acid,RNA)或蛋白质(Protein)也可能肩负相同的职责。
相比于由两条链互相配对形成的 DNA,新冠病毒的单链 RNA 基因组,产生突变或变异的概率更高。
 不同类型病毒突变率比较 | Sanjuán, R., Domingo-Calap, P., 2016.
不同类型病毒突变率比较 | Sanjuán, R., Domingo-Calap, P., 2016.
一年多的时间在人类看来不算太久,可对病毒而言就截然不同。新冠病毒大量的复制和繁殖,意味着数不胜数的变异在悄然发生,其中发生在关键基因上的“有利”变化,则可能让它们更加强大。
变异的新冠病毒会变强?冠状病毒主要感染禽类和其他哺乳动物,但有一些越过了其他哺乳动物—人类之间的屏障,逐渐发展为人畜共患的传染病;而从其他动物到人之间的跃迁背后,正是变异和进化在“作祟”。
此前已经确定的、可感染人类的冠状病毒有6种:HCoV-229E、HCoV-OC43、SARS-CoV、HCoV-NL63、HCoV-HKU1 和 MERS-CoV;在过去的这段时间里又增加了一种——新型冠状病毒(SARS-CoV-2)。
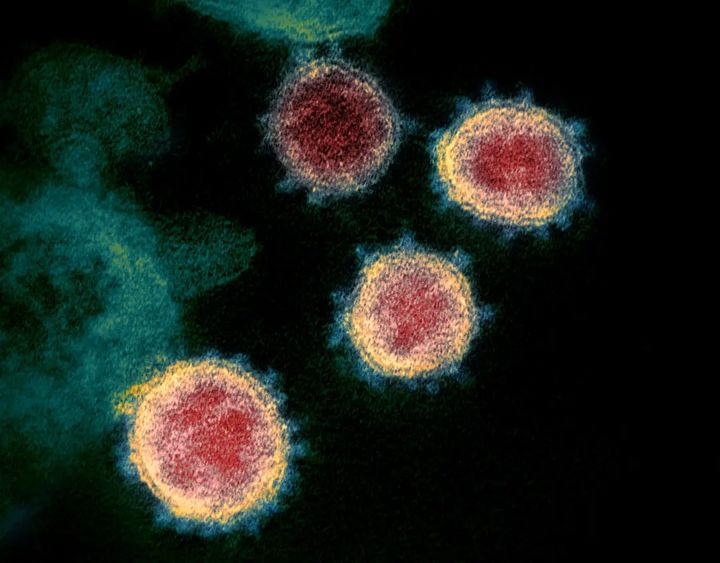 电子显微镜下染色后的新冠病毒 | NIAID
电子显微镜下染色后的新冠病毒 | NIAID
冠状病毒的基因组主要编码四种结构蛋白:刺突蛋白(S),核衣壳蛋白(N),膜蛋白(M)和包膜蛋白(E);这些蛋白质在形成病毒颗粒的结构时起到至关重要的作用,有些也会参与复制周期等其他方面。
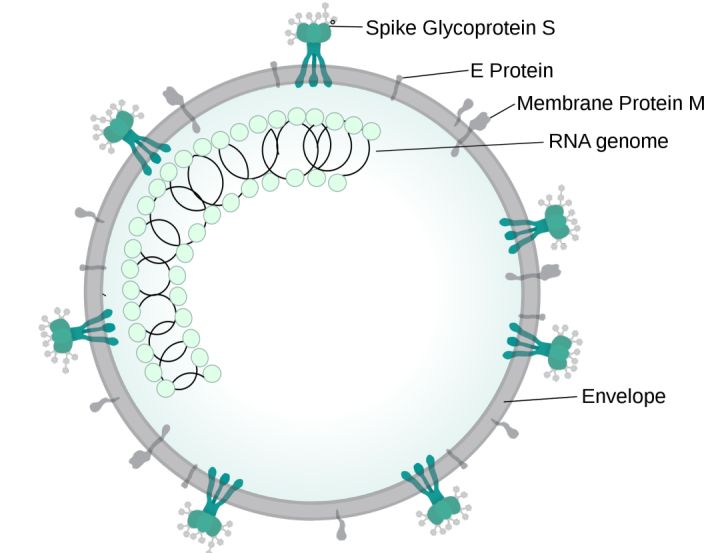 新冠病毒的主要结构 | SPQR10
新冠病毒的主要结构 | SPQR10
其中,很大程度上,决定冠状病毒是否能够感染人类、甚至进一步“人传人”的是刺突蛋白(S蛋白)。
以 SARS 冠状病毒为例,其 S 蛋白的受体结合域中,仅仅几个突变(N479L 和 T487S)就足以显着增加与人细胞表面受体(ACE2)的亲和力。
在论文或新闻中出现的突变类型格式为“突变前的氨基酸代号-位置编号-突变后的氨基酸代号”,每一种氨基酸都有一个对应的字母,而数字是指在这个蛋白质/多肽的氨基酸链上的位置。例如 N479L 是指在这个蛋白质上,第479个氨基酸由天冬酰胺(N)突变为亮氨酸(L)。而中东呼吸综合征冠状病毒(MERS-CoV)不仅仅需要突变帮助它结合人细胞表面的受体(DPP4),还需要 S 蛋白中另外两个突变(S746R 和 N762A)的帮助,使其能够被来自人的蛋白酶切割激活,从而让病毒进入人细胞。
这一次在英国被发现的新冠病毒变异毒株 B.1.1.7,也包含了 S 蛋白上的关键氨基酸突变——N501Y。结合目前英国新冠疫情的增长情况来看,这一变异毒株在进入呼吸道等器官的细胞、感染人类的能力上可能增强了。
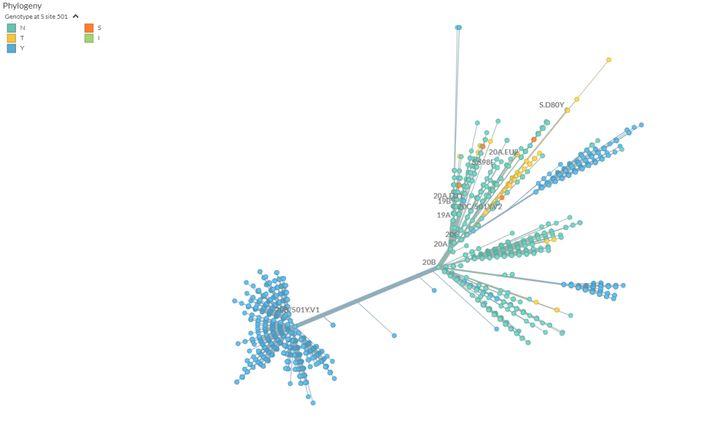 新冠病毒 S 蛋白第501位氨基酸的变异情况 | emmahodcroft/ncov_cluster
新冠病毒 S 蛋白第501位氨基酸的变异情况 | emmahodcroft/ncov_cluster
只不过包括 B.1.1.7 在内的各种变异类型,具体是如何加强其传染能力、会不会由突变提升致病性或临床症状的严重程度,以及针对这些病毒蛋白研发的疫苗会不会失效等问题,还需要更多实验室内或临床上的数据和细节才能够得出结论。
博弈的终点会怎样?对于人类而言,要在进化和选择的过程中发生结构或生理上的变化需要数万年;但对于小小的病毒来说,过去一年多的时间里,就足够发生不少改变。
而在这场博弈当中,新冠病毒正在经历被人类影响的自然选择,这也是为什么大多数时候人类只会发现更危险的变异株。因为那些具备无关紧要或其他功能的突变,在人类隔离、治疗和疫苗的选择压力下会慢慢消失。
所以,这场博弈的终点就取决于人类能否用正确、有效的隔离阻断病毒的传播,药物和疫苗研发的速度能否赶上病毒变异的脚步。
也就是人类的决心和智慧。
参考资料
Kai Kupferschmidt (2021). Viral mutations may cause another ‘very, very bad’ COVID-19 wave, scientists warn. Science.
Sanjuán, R., Domingo-Calap, P (2016). Mechanisms of viral mutation. Cell. Mol. Life Sci. 73, 4433–4448.
Snijder EJ, Decroly E, Ziebuhr J (2016) The nonstructural proteins directing coronavirus RNA synthesis and processing. Adv Virus Res 96:59–126
Li F (2008) Structural analysis of major species barriers between humans and palm civets for severe acute respiratory syndrome coronavirus infections. J Virol 82:6984–6991.
Yang Y, Liu C, Du L, Jiang S, Shi Z, Baric RS, Li F (2015) Two mutations were critical for bat-to-human transmission of middle east respiratory syndrome coronavirus. J Virol 89: 9119–9123.
Adriaan H. de Wilde, Eric J. Snijder, Marjolein Kikkert and Martijn J (2017). van Hemert. Host Factors in Coronavirus Replication. Current Topics in Microbiology and Immunology.
Shin, M.D., Shukla, S., Chung, Y.H. et al (2020). COVID-19 vaccine development and a potential nanomaterial path forward. Nat. Nanotechnol. 15, 646–655.
Huang, Y., Yang, C., Xu, Xf. et al (2020). Structural and functional properties of SARS-CoV-2 spike protein: potential antivirus drug development for COVID-19. Acta Pharmacol Sin 41, 1141–1149.
Mittal A, Manjunath K, Ranjan RK, Kaushik S, Kumar S, Verma V (2020). COVID-19 pandemic: Insights into structure, function, and hACE2 receptor recognition by SARS-CoV-2. PLoS Pathog.16(8):e1008762.
本文链接:https://www.bjjcc.cn/kepu/16217.html,文章来源:科普之家,作者:biokiwi,版权归作者所有,如需转载请注明来源和作者,否则将追究法律责任!
